In vivo self-assembled nano-PROTAC for the dual degradation of AR and HSP90 to overcome castration-resistant prostate cancer resistance.
研究背景
去势抵抗性前列腺癌(CRPC)对第二代雄激素靶向疗法存在耐药问题,临床治疗面临挑战。本文基于体内自组装纳米技术,设计PSMA靶向的nano - PROTAC,旨在评估其克服CRPC耐药性的潜力。
方法速览
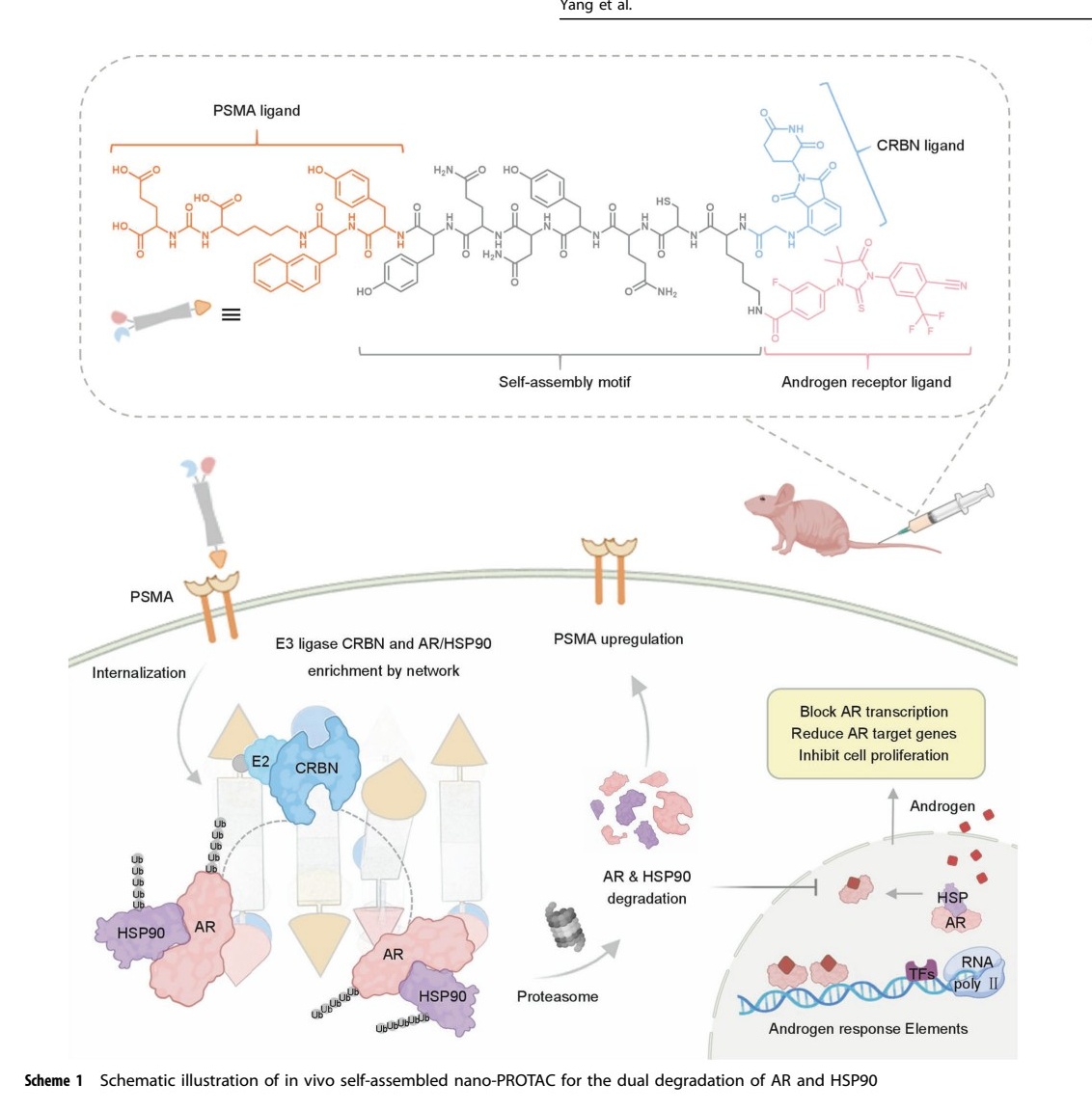
- 设计与验证:模块化设计nano - PROTAC,含PSMA靶向配体、自组装肽、AR结合基团和E3连接酶配体。
- 细胞评估:用共聚焦激光扫描显微镜和扫描电子显微镜评估细胞内化和分布。
- 蛋白分析:通过Western Blot和免疫荧光分析AR和HSP90降解情况。
- 体内实验:在荷瘤小鼠模型评估生物分布和抗肿瘤效果。
主要发现
- 高效降解蛋白:在22Rv1细胞模型中,nano - PROTAC能降解80%的AR蛋白、65%的HSP90蛋白和74%的AR剪接变异体AR - V7蛋白,抑制CRPC细胞生长。
- 体内疗效显著:恩杂鲁胺耐药的异种移植肿瘤小鼠模型中,nano - PROTAC治疗组肿瘤生长抑制值达78%,中位生存期延长15天。
- 剂量依赖与持续效应:nano - PROTAC在22Rv1细胞中呈浓度依赖性降解AR蛋白,40 μM时达80%降解率,96小时内维持超99%蛋白敲低率。
- 选择性和特异性好:PSMA敲低的22Rv1细胞中,nano - PROTAC脱靶效应小,目标特异性优越。
- 高效降解AR - V7:降解AR - V7效率比P - AR高66%,机制可能是抑制HSP90促进AR - V7泛素化清除。
- 细胞毒性低:在PSMA低表达的正常RWPE - 1细胞中细胞毒性可忽略,细胞活力超90%。
- 肿瘤积累佳:荷瘤小鼠模型中,nano - PROTAC 2小时内肿瘤选择性积累,24小时内残留信号78%,优于传统PROTAC。
- 抗肿瘤效果好:22Rv1异种移植肿瘤模型中,肿瘤体积抑制率65%,中位生存期48天,优于对照组。
总结展望
nano - PROTAC通过多靶点降解、自组装纳米结构和精准选择性,有效克服CRPC耐药性。不过,目前研究主要针对PSMA阳性和AR阳性的CRPC,长期安全性也需进一步评估。

