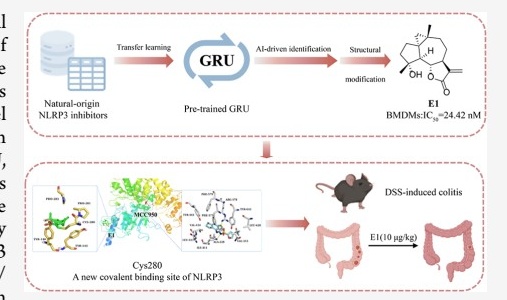
AI-Driven Transfer Learning and Generative Model (TransGenGRU) Enables the Drug Discovery of Novel Natural Guaianolide Sesquiterpene Derivatives as Potent NLRP3 Inhibitors
研究背景
NLRP3炎性体在先天免疫中调节促炎细胞因子成熟。虽有多种天然产物具NLRP3抑制活性,但因生物活性、稳定性和药代动力学问题限制开发。为此,研究人员提出AI模型(TransGenGRU)生成新的NLRP3抑制活性天然产物。
方法速览
- 建立TransGenGRU模型,用转移学习生成具NLRP3抑制活性的新型天然产物。
- 化学合成候选化合物,在BMDMs和PBMCs中评估NLRP3抑制活性。
- 用CETSA、SIP和SPR实验验证E1与NLRP3结合,质谱分析确定结合位点。
- 在DSS诱导的结肠炎和MSU诱导的腹膜炎小鼠模型中评估E1抗炎效果。
- 评估E1的代谢稳定性和药代动力学特性。
主要发现
- 广谱抑制NLRP3激活:E1在BMDMs中IC50值为24.42 nM,能剂量依赖性抑制caspase - 1表达和IL - 1β释放,还抑制MSU晶体和尼日里辛诱导的NLRP3激活。
- 选择性抑制:E1对AIM2、NLRC4和NLRP1炎性体激活无抑制作用。
- 抑制复合体组装:E1能浓度依赖性抑制NLRP3/pro - caspase - 1/ASC复合体组装。
- 直接结合NLRP3:实验证实E1可直接与NLRP3结合,结合常数为1.138 × 10^ - 7 mol/L。
- 共价不可逆结合:质谱显示E1与NLRP3的Cys280共价结合,还原α,β - 不饱和内酯基团后,抑制活性显著下降。
- 体内抗炎效果:在DSS诱导的结肠炎和MSU诱导的腹膜炎小鼠模型中,口服E1改善症状、降低相关指标。
总结展望
研究首次用AI技术生成具NLRP3抑制活性的新型天然产物E1。它通过独特共价不可逆方式与NLRP3结合,在多种炎症模型中验证抗炎效果,有潜在临床应用价值。不过,E1药代动力学性质待优化,还需更多临床前研究验证安全性和有效性。